29. lecke
A 29. lecke, „A koncepció az alapon,” persze „Chemistry for Dummies” megismerkednek egy új osztály a vegyi anyagok - bázisok, valamint megtudjuk, egy új típusú kémiai reakciók - csere reakciók.

Mint már tudjuk, a kölcsönhatás az aktív fémek és oxidok képződnek vízzel bázissal - vegyületek, amelyek nem tartoznak sem a híres még osztályok oxidok, sók vagy savak.
Bázisok, mint összetett anyagok
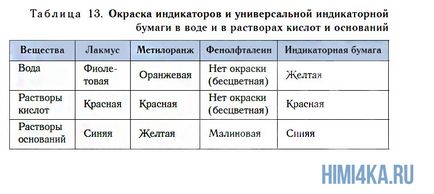
Mi teszteltük az indikátoroldat reakciójával kapott CaO kalcium-oxid vízzel. Ahhoz, hogy ez a mi adjunk hozzá 1-2 csepp metilnarancs oldatot. az oldat színe megváltozott narancssárgáról sárgára (ábra. 111).

Ez azt jelzi, hogy ez a megoldás nincs sav, és néhány új anyag, megváltoztatja a színét az indikátor. Mint a kalcium-oxid vízzel reagál és bizonyos egyéb oxidok, mint a nátrium-oxid Na2 O:
A reakciót a kalcium-oxid és a nátrium-vízzel képződött anyag Ca (OH) 2 és NaOH. Ezek hasonlóak, hogy hatóanyagként a fématomok, és az OH-csoport. gidroksogrupp nevezik (a görög szó „Hydor”, ami azt jelenti, „víz”). Ezek az anyagok osztályába tartoznak a bázisok.
Grounds - komplex anyagok, amelyek fém-atomok és gidroksogrupp.
Vegyérték gidroksogrupp egységét. Ennek tudatában, hogy könnyen, hogy minden olyan bázist képlet: száma OH-csoportok a bázis képletű mindig vegyértékével egyenlő a fématom. például:
Ugyanakkor a bázis a következő képlet szerint könnyen meg tudja határozni a fém vegyértékétől atomok abban foglalt - ez jelen van képletű chislugidroksogrupp bázis. Például, egy bázis képletű Fe (OH) 2 két gidroksogrupp tehát, a vegyérték vas atomok ez a vegyület a II, és az alapja Cr (OH) 3 a vegyértékével egyenlő a króm atomok III.
Mint jól ismert, mint az alap? Ismeretes, hogy a termékek a vegyületek vízzel anyagok az úgynevezett hidrátok. Ha víz csatlakoztatott fém-oxidok keletkeznek, hidraulikus Ata s fém-oxid. vagy rövidített fém-hidroxidok. Ezért a Ca szer (OH) 2 és NaOH, kölcsönhatásából képződik a kalcium- és nátrium-oxid vízzel, az úgynevezett „kalcium-hidroxid„és a”nátrium-hidroxid".
Vízoldhatóság alapon vannak osztva oldható és oldhatatlan. bázisok vízben oldódik nevezzük lúgok. Ezek közé tartoznak a kálium-hidroxid, nátrium-hidroxid, Ca (OH) 2. Ba (OH) 2 és mások.
Detect jelenlétében vízben oldható bázis (alkálifém) lehet az indikátor színváltozás. Emellett híres lakmusz metilnarancsoldatot, és erre a célra, akkor használjon egy másik mutató - fenolftalein. Ez nincs színe a vízben, és a savas oldatot, de alkália jelenlétében, ez a mutató van színezve a bíbor szín (lásd. Ábra. 111, pl. 13).
semlegesítési reakció
Amint látható, a vízoldható bázisok - lúgok - könnyen kimutatható a mutatók. Azonban, ha egy oldat nátrium-hidroxid, nátrium-hidroxid hozzáadásához fenolftalein, majd sósav, az első bíbor elszíneződés jelent meg a sav hozzáadása után eltűnik (ábra. 112).

Ez azt jelzi, hogy a sav tönkretenné vagy semlegesítse a bázist. A reakció a sav és a bázis áramló ebben az esetben az úgynevezett semlegesítési reakció:
semlegesítési reakciót - a reakció között a bázis és a sav, így a képződött sót és a vizet.
semlegesítési reakció nem tartozik az egyik a híres még típusú reakciók (bomlástermékek helyettesített). Ez a reakció egy új típusú - kicserélődési reakció.
Az Exchange reakciókat nevezzük közötti reakciók komplex anyagok, amelyben kicserélik a alkotóeleme.
Az alap fémből áll atomok és gidroksogrupp és sav - hidrogénatom vagy savmaradék. A reakciót a kiindulási anyagok kicserélt alkatrészek hozzá (ábra. 113):
Rövid lecke következtetéseket:
- Grounds - komplex anyagok, amelyek fém-atomok és gidroksogrupp.
- Közötti reakció a sav és bázis, amelyben a képződött sót és a vizet, az úgynevezett semlegesítési reakció.
- Metatézis - közötti reakció összetett anyagok, mint amelynek eredményeként kommunikálnak összetevők.