A vízgőz, a blog energia
Köztes halmazállapot között az állam egy igazi gáz és folyadék úgynevezett gőz vagy csak gőzt. Az elpárologtatott folyadék egy fázis átmenet az egyik állapotból a másikba. A fázisátalakulás megfigyelt hirtelen megváltozása fizikai tulajdonságai az anyag.
Ilyen fázisátalakulások folyékony forralási folyamat bevezetésével nedves telített gőz és annak későbbi áttérés mentes nedvesség a száraz telített gőzt főzési eljárással vagy fordított páralecsapódás.
Az egyik fő tulajdonságai a száraz telített gőz, hogy a további hőközléssel rá növekedéséhez vezet a gőz hőmérsékletét, azaz a átmenet állapotában túlhevített gőz, és a hő eltávolítását - .. Az átmenet az állam a nedves gőz. az
Phase víz állapotai
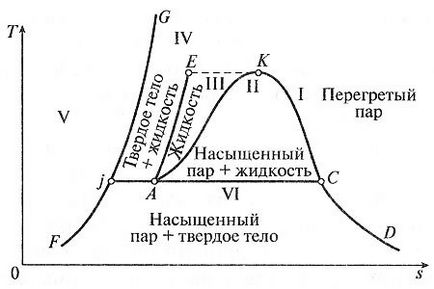
1. ábra: A fázisdiagramja vízgőz T, s koordináták.
Oblasti - gáz halmazállapotú (túlhevített gőzt a tulajdonságait egy valódi gáz);
OblastII - egyensúlyi állapotban a víz és telített gőz (kétfázisú állapotban). Terület II néven párologtatás régióban;
OblastIII - folyékony állapotban (víz). Kerület III korlátozott izoterma EK
OblastIV - egyensúlyi állapot a szilárd és folyékony fázisok;
Region III, II és I elválasztva határvonalak AK (bal vonal), és a KD (jobb vonal). Összesen K pont a határvonalak AK KD és a különleges tulajdonságokkal nevezik kritikus pont. Ezen a ponton paraméterek PKR, VCR és a TCR. amelyben a forró víz áthalad a túlhevített gőz, átadva a kétfázisú régióban. Következésképpen, a víz nem létezhet feletti hőmérsékleten T c.
A kritikus pont K-nak a paramétereket:
Az értékek p, T, V, és s mind a határoló vonalak vannak speciális táblázatok termodinamikai tulajdonságainak vízgőz.
A folyamat gztermelést vízből
2. és 3. ábra mutatják, a víz fűtési folyamat forrásig, párolgás és túlhevítő a p, v - és a T, s-diagram.
A kezdeti állapotban a folyékony víz nyomás alatt p0 és amelynek hőmérséklete 0 ° C-on, az ábrázolt grafikonok p, v és T, S pont. Amikor hőbevitel p = const, a hőmérséklet növekszik, és növekszik fajlagos térfogata. Egy bizonyos ponton, a víz hőmérséklete eléri a forráspontot. Ebben az állapotban a kijelölt pont b. A további hőbevitel párologtatás kezdődik erős volumen növekedése. Ez képezi egy kétfázisú közeg - víz és a gőz, az úgynevezett nedves telített gőz. A keverék hőmérséklete nem változik, mivel a hő fogyasztott elpárolgását a folyékony fázis. párologtatás folyamat ebben a szakaszban az a izobár-izoterm és jelöljük az ábrán, mint BC része. Aztán, valamikor, a víz gőzzé alakul át, említett száraz telített. Ezt az állapotot a rajzon c pont.
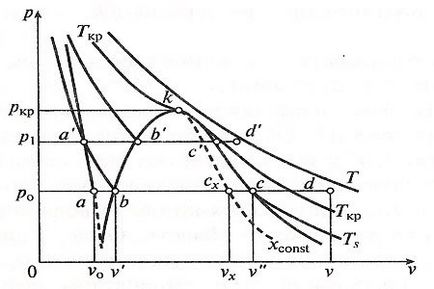
2. ábra: Diagram p, v víz és gőz.
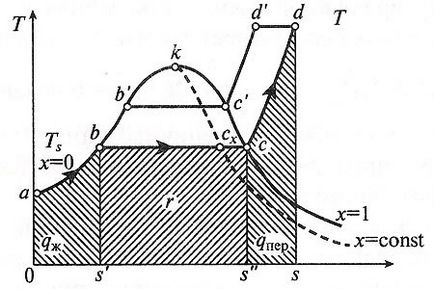
3. ábra diagram T, S a víz és a vízgőz.
A további hőbevitel növeli a gőz hőmérséklete fog folyni és túlhevítő folyamat c - d. D pont van kijelölt állapotban túlhevített gőz. A távolság d pont pont függ a hőmérséklettől a túlhevített gőz.
Az indexelés jelölésére mennyiségeket az egyes államok a víz és gőz:
- értéket a alsó index „0” kifejezés a kezdeti állapot a víz;
- értéket a utótag „„”jelenti azt a vizet, forrásig melegítjük (telítési);
- értéket a utótag „„”kifejezés a száraz telített gőzt;
- index értéke «x» utal, hogy a nedves telített gőzt;
- nélküli érték egy index utal túlhevített gőz.
A folyamat a párolgás nagyobb nyomás p1> p0 lehet jegyezni, hogy egy pont ami a kezdeti állapotban a víz 0 ° C-on, és az új nyomás közel azonos függőleges vonal, mivel a fajlagos térfogat víz szinte független a nyomástól.
B pont „(az állam a víz telítési hőmérséklet) jobbra tolódik által p, v és -diagram emelkedik T, s -diagram. Ez azért van, mert egy a nyomás növekedésével nő a telítési hőmérséklete, és így, egy adott mennyiségű vízzel.
Pont c „(az állam száraz telített gőz) balra tolódik, vagyis. K. A nyomás növeli a fajlagos térfogata gőz csökken annak ellenére, hogy a hőmérséklet emelkedését.
Vegyület több B és C pontok különböző nyomásokon biztosít egy alsó és egy felső határoló görbék ak és a KC. P, v-diagram látható, hogy a nyomás közötti különbség fajlagos térfogat V „és V„csökken, és egy bizonyos nyomást nullává válik. Ezen a ponton, az úgynevezett kritikus határvonal görbék ak és kc. Állami pontnak megfelelő k. Ez az úgynevezett kritikus. Ez jellemzi az a tény, hogy amikor azt és a vízgőz fajlagos térfogat azonos vagy eltérő tulajdonságokkal egymástól. Region fekvő ívháromszögének BKC (p, v -diagram), megfelel a nedves telített gőz.
Az állam a túlhevített gőzzel ábrázolt pont felett fekvő felső határa görbe kc.
A T, s -diagram terület 0abs' megfelel a hőmennyiség melegítéséhez szükséges a folyékony víz a telítési hőmérséklet.
Száma Összefoglalva hő, J / kg, egyenlő a párolgási hőt R, fejezi ki egy olyan terület s'bcs, és a hozzá képest:
A hőmennyiség során összegezve túlhevített gőz által képviselt terület s „CD-ket.
A T, s -diagram látható, hogy a nyomás csökken és a párolgási hőt a kritikus pont lesz nulla.
Normális, T, S -diagram használt elméleti kutatások, hiszen a gyakorlati haszna van nagyon megnehezítette az a tény, hogy a hőmennyiség kifejezett területeken görbe vonalú formák.